Preimplantačné embryo (blastocysta) nie je iba sférickým zhlukom zárodočných buniek, z ktorého vzniká nový život. Predstavuje autonómny organizmus, ktorý je schopný odolávať, brániť sa a prispôsobovať sa okolitému prostrediu, či už vnútornému (obezita, cukrovka), alebo vonkajšiemu (stres, fajčenie, vplyv rôznych chemických látok). Je to bojovník, ktorý sa snaží prežiť.
Blastocysta predstavuje skoré embryonálne štádium cicavcov. Vzniká na 4. až 7. deň po oplodnení a je výsledkom intenzívneho delenia embryonálnych buniek, blastomér. Pozostáva z trofoblastu, vonkajších buniek lemujúcich blastocystu, a z embryoblastu, pólovo umiestnených embryonálnych buniek, ktoré sú základom pre vývin budúceho jedinca.
Dôležitý začiatok
Dutinu blastocysty označujeme ako blastocel. Povrch blastocysty ohraničuje tzv. zona pellucida, ktorá zohráva najväčšiu úlohu pri selekcii spermií pri oplodnení vajíčka. Po preniknutí vhodnej spermie dochádza k zmene štruktúry tohto proteínového obalu, a tým dôjde k obmedzeniu ďalšieho prieniku spermií. Blastocysta sa voľne pohybuje v dutine maternice, postupne rastie a zväčšuje sa. Zona pellucida sa postupne stenčuje, dochádza k jej prasknutiu a tzv. hatchingu blastocysty (vyliahnutie).
Takáto obnažená blastocysta je na 6. až 17. deň po oplodnení pripravená uhniezdiť sa do steny maternice (v závislosti od živočíšneho druhu). Trofoblast začína uvoľňovať enzýmy, ktoré rozrušujú povrch endometria (vnútornej výstelky maternice), a tým pomáhajú k uhniezdeniu blastocyty embryoblastovým pólom do steny maternice. Po zahniezdení sa z trofoblastu vyvinie placenta, ktorou je vyživovaný plod, a z embryoblastu telo samotného jedinca.
Nástrahy a selekcia
Obdobie od oplodnenia po zahniezdenie v maternici je plné nástrah a predstavuje určitú selekčnú periódu, ktorú prežijú iba bezchybne vyvinuté embryá. Odborná literatúra popisuje, že nie každé oplodnenie vajíčka vedie ku gravidite a k donoseniu zdravého jedinca. V priebehu preimplantačného vývinu dochádza vplyvom nepriaznivých vývinových podmienok alebo v dôsledku náhody k rôznym poškodeniam embryonálnych buniek. Niektoré poškodené bunky je embryo schopné zreparovať, iné zanikajú, najčastejšie procesom zvaným apoptóza.
Apoptóza je fyziologický, geneticky riadený proces autodeštrukcie. Apoptotické bunky sú buď vylúčené z embrya, alebo prehltnuté a strávené okolitými bunkami. Vtedy vysielajú tzv. eat me (zjedz ma) signál, ktorým informujú susedné embryonálne bunky, že sú vhodné na elimináciu prostredníctvom fagocytózy.
Poznanie pomôže prežiť
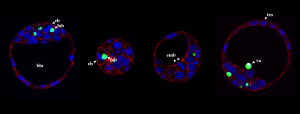
V súčasnosti môžeme pomocou vhodného modelového organizmu (preimplantačný vývin je veľmi dobre popísaný pri myšiach), výberu fluorescenčných farbiacich techník a vhodného zobrazovacieho zariadenia – napr. konfokálnej mikroskopie – pozorovať osud apoptotických embryonálnych buniek. Apoptotické bunky musia byť eliminované, lebo inak by mohli ohroziť homeostázu a vitalitu blastocýst. V dospelom organizme dochádza k fagocytóze apoptotických buniek prostredníctvom makrofágov. Apoptotické embryonálne bunky sú fagocytované susednými embryonálnymi bunkami tzv. eferocytózou. Vedci zistili, že aj takáto málo diferencovaná bunka, ako je embryonálna, dokáže rozpoznať apoptotickú embryonálnu bunku, a následne ju pohltiť. Tým predchádza jej samovoľnému rozpadu a vyliatiu toxického bunkového obsahu do vonkajšieho prostredia. Je dokázané, že preimplantačné embryo disponuje mechanizmami, ktorými odstraňuje poškodené embryonálne bunky, a tým je schopné regulovať svoj vývin a byť na pozore.
Poznanie fyziologických dejov, ktoré prebiehajú v blastocyste, je veľmi dôležité pre klinickú prax. Ďalším pozorovaním a bádaním sa možno dopracujeme k poznaniu, ktoré nám umožní regulovať prežívanie a predchádzať zániku preimplantačných embryí, a tým riešiť niektoré problémy s neplodnosťou v humánnej a veterinárnej reprodukčnej medicíne.
PhDr. Jozef Pisko, PhD.
Ústav fyziológie hospodárskych zvierat
Centrum biovied SAV, v. v. i.
APVV-22-0071, VEGA 2/0041/23
Článok vznikol v spolupráci s platformou Mladí vedci SAV.


