Aj napriek pandémii spôsobenej ochorením covid-19, ktorá je v súčasnosti hlavnou témou v odborných či menej odborných médiách, kardiovaskulárne ochorenia naďalej zostávajú v rozvinutých krajinách hlavnou príčinou chorobnosti a úmrtnosti.

Netreba preto zabúdať, že štúdiu mechanizmov vedúcich ku kardioprotekcii treba venovať veľkú pozornosť. Hoci v súčasnosti existujú medicínske technológie a terapie, ktoré sú schopné znížiť poškodenie spôsobené kardiovaskulárnymi ochoreniami, molekulárne mechanizmy na úrovni subcelulárnych systémov sú ešte vždy málo objasnené.
Adaptácia srdcového svalu
Jednou zo základných vlastností srdca je schopnosť adaptácie a remodelácie. Dôsledkom vystavenia myokardu (srdcovej svaloviny) opakujúcim sa záťažiam sa srdce adaptuje na patologickú alebo fyzickú záťaž a prispôsobí sa jeho zvýšeným energetickým požiadavkám. Typickým príkladom adaptácie srdca prejavujúcim sa u profesionálnych športovcov je hypertrofia svaloviny ľavej komory, ktorá je zodpovedná za pumpovanie krvi do celého tela. Podobným spôsobom sa srdce dokáže predpripraviť tzv. preconditioningom, teda opakovaným vystavením krátkodobej patologickej záťaži, akou je napríklad ischemicko-reperfúzne poškodenie, na nasledujúcu záťaž a rozsah poškodenia nebude taký závažný.
Srdcová remodelácia okrem zmien na úrovni štruktúr srdcového tkaniva zahŕňa štruktúrne a funkčné zmeny na subcelulárnej úrovni. Obzvlášť významným koncovým efektorom zapojeným v procesoch adaptácie a endogénnej ochrany myokardu sú mitochondrie.
Energetická továreň bunky
Mitochondrie sú najdôležitejším producentom energie. V ľudskom srdci dokážu za jeden deň vyprodukovať až 6 kg molekúl adenozíntrifosfátu (ATP má kľúčovú úlohu pri prenose energie v bunke). Toto množstvo energie je potrebné na udržanie kontraktilnej funkcie myokardu a umožňuje vykonať okolo 100 000 úderov denne. Okrem toho tieto organely zodpovedajú za bazálne metabolické procesy či za udržanie iónovej homeostázy, preto má ich dysfunkcia za následok viacero závažných ochorení vrátane kardiovaskulárnych. Významnou úlohou srdcových mitochondrií v procesoch endogénnej ochrany je ich účasť na procesoch kompenzácie pri zvýšených energetických nárokoch.
V súčasnosti je jedným z hlavných cieľov výskumu v oblasti kardioprotekcie vývoj stratégií zameraných na zachovanie energetickej rovnováhy myokardu. Mitochondriálna dysfunkcia sa javí ako efektívny cieľ kardioprotektívnej terapie, ktorej prejavom je zabezpečenie energetickej udržateľnosti a zlepšenie prežívania myokardu.
Mitochondriálny proteóm
V tejto súvislosti sa aj my v našom pracovnom tíme v laboratóriu hmotnostnej spektrometrie a fluorescenčnej spektroskopie Ústavu pre výskum srdca Centra experimentálnej medicíny SAV venujeme protektívnej regulácii signálnych dráh srdcových mitochondrií v podmienkach kyslíkovej deprivácie, hypoxie a ischemickej choroby srdca. Zaoberáme sa objasnením molekulárnych mechanizmov, ktoré vedú k záchrane srdca v stave záťaže, predovšetkým na úrovni modulácie mitochondriálnych membrán a proteínov.
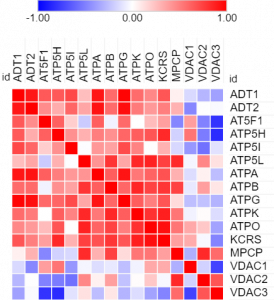
Identifikácia proteínov a potenciálnych biomarkerov sa ukazuje byť vhodnou voľbou na určenie zmien súvisiacich s ochoreniami myokardu a ich strategickou terapiou. Pomocou moderných a perspektívnych metodických prístupov hmotnostnej spektrometrie sledujeme proteomické zmeny na úrovni srdcových mitochondrií, ktoré nám vedia poskytnúť cenné informácie o patologických, rovnako aj o adaptačných a funkčných procesoch v myokarde. Analýzy mitochondriálneho proteómu nám umožňujú lepšie porozumieť tejto komplexnej organele a jej rozmanitým funkciám.
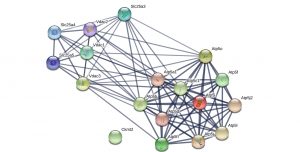
Okrem identifikácie a kvantifikácie proteínov sa venujeme štúdiu a pochopeniu významu proteínovo-proteínových interakcií, ktoré sú veľkým prínosom pri definovaní mitochondriálneho proteómu. Práve poznanie proteínovo-proteínových interakcií môže byť základom pre vývoj nových terapeutík. Takýto druh štúdií je najmä v súvislosti s patológiami nedostatočný, a preto implementáciou proteomiky prináša naša práca cenné poznatky o adaptačných mechanizmoch účinných v procesoch ochrany myokardu.
Text a foto Mgr. Natália Andelová
Ústav pre výskum srdca
Centrum experimentálnej medicíny SAV
Článok vznikol v spolupráci s platformou Mladí vedci SAV.


